Índice ELSA en la evaluación de síntomas de pacientes con esofagitis eosinofílica
Rodríguez-Sánchez J (1), Gómez Torrijos E (2), López Viedma B (1), Martín Dávila F (3), González López L (3), Olmedo Camacho J (3)
1 Sección de Aparato Digestivo. 2 Sección de Alergología. 3 Servicio de Anatomía Patológica. Hospital General Universitario de Ciudad Real.
Correspondencia:
Dr. Joaquín Rodríguez Sánchez
Sección de Aparato Digestivo. Hospital General Universitario de Ciudad Real.
C/ Obispo Rafael Torija s/n Ciudad Real (Spain).
Tel.: 926 278 000 Ext 79606.
Email: joarosa@sescam.jccm.es
ABSTRACT
Introducción. Hasta la fecha no se dispone de herramientas clínicas específicas de esofagitis eosinofílica para evaluar la actividad clínica de la enfermedad, usándose diferentes escalas de disfagia o acalasia para este fin. Dado que se trata de un proceso con actividad clínica intermitente, es de interés crear Scores específicos para la enfermedad.
Objetivos. Evaluar la eficacia del Índice ELSA para monitorizar la actividad clínica de la esofagitis eosinofílica.
Métodos. Análisis prospectivo de la eficacia de Índice ELSA en pacientes sometidos a tratamiento con omeprazol 40 mg/24 h + dietas: Dieta de exclusión selectiva según tests de alergia (SED) y dieta de exclusión de 6 familias de alimentos (SFED). Determinando la puntuación del score pre-tratamiento y pos-tratamiento. El rango de Índice ELSA es (0-70 puntos) siendo un sumatorio de 7 ítems puntuados por el paciente (del 0 al 10) en función de la severidad: (A) dificultad para deglutir, (B) dolor torácico con la deglución, (C) Nudo en el cuello/pecho, (D) Regurgitaciones, (E) Sensación de pirosis, (G) Impactaciones con sólido. Se evaluó las diferencias en las puntuaciones en pacientes respondedores y no respondedores, pre y post tratamiento. Las puntuaciones basales (pretratamiento) fueron comparadas con las obtenidas por un grupo de 20 controles sanos.
Resultados: 20 pacientes (80% varones) con edad media 32±12.38. Pico de eosinófilos en biopsias al diagnóstico: 36,05 eo/hpf. Respuesta global a IBP+dietas (SED+SFED) 13/20; 65%. Índice ELSA: EoE vs. Control (18.70 vs 3.81; p<0.000). (A) es el síntoma con mayor puntuación (6.35/10), siendo (B) el menos puntuado (2/10). Índice ELSA predieta: Respondedores (R) vs. no respondedores (NR) (30.38 vs 26.86; p=0.53). Índice ELSA en R: Pretratamiento vs. Posttratamiento (30.38 vs. 5.08; p<0.000). ELSA en NR: Pretratamiento vs. Posttratamiento (26.86 vs. 14,14; p=0,01). En R, (A) es el síntomas que mejora más (6,38 vs. 0,92; p=0,001). A diferencia de R, en NR tan sólo mejoran de forma significativa (A) (6,29 vs. 2,71; p=0,01) y (C) (6 vs. 3,57; p=0,04). No se encontró correlación entre la puntuación del Score y los valores de eosinófilos en suero, ECP en suero, IgE total, eosinófilos/hpf en las biopsias pre y post tratamiento.
Conclusión. Índice ELSA es una herramienta eficaz en el seguimiento de la actividad de la esofagitis eosinofílica, siendo a la vez capaz de cuantificar la influencia cada uno de los síntomas sobre el espectro clínico de la enfermedad. La puntuación de ELSA no se correlacionó con parámetros de actividad del eosinófilo.
INTRODUCCIÓN
La esofagitis eosinofílica (EoE) es un trastorno cada vez más frecuente en nuestro medio (1), en el que para su diagnóstico debemos demostrar la presencia de más de 15 eosinófilos (eo)/campo de gran aumento (cga) (x40) en las biopsias de esófago, así como una clínica compatible de disfunción esofágica de curso fluctuante (2) que varía según la edad de los pacientes (3). La disfagia es el síntoma más frecuente en población adulta (4, 5), mientras que en edad pediátrica los vómitos y la pérdida de peso son las manifestaciones más frecuente (6). En los últimos años, se han publicado diferentes scores de síntomas en pacientes pediátricos que intentan cuantificar la severidad de la afectación clínica, y a su vez correlacionarla con los hallazgos histológicos. Así Pemtiuk y cols.(7) desarrollaron el non-validated Pediatric Eosinophilic Esophagitis Sympton Score (PEESS versión 1.0), donde demostraron como pacientes no tratados presentaban una puntuación mayor en el score que aquellos que recibieron tratamiento (p=0,045), detectando correlación entre el número de (eo) en la biopsia y la puntuación del test. Recientemente Franciosi y cols. han publicado la versión validada de este Score (PEESS v2.0) (8). Relacionando la EoE con la enfermedad por reflujo gastroesofágico (ERGE) en pacientes pediátrico, Acebes y cols. publicaron un score de síntomas donde EoE y ERGE obtenían mayor puntuación que un grupo control (p=0,001). Ya en población adulta, existen diferentes estudios que intentan predecir la presencia de EoE, así Dellon y cols. (9) observaron que la edad (< 18años) y síntomas de disfagia, se comportaban como factores predictores de EoE, hecho que nosotros constatamos en nuestro medio (10). Recientemente, Mulder y cols. (11) han comprobado como: sexo masculino, disfagia, historia previa de impactaciones y ausencia de pirosis son capaces de predecir la presencia de EoE frente a la ERGE (AUC=0,85). Por lo tanto, existe una clara evidencia de que la EoE presenta un espectro clínico específico. Dicha constelación de síntomas, tiene un claro impacto sobre la calidad de vida, lo cual ha sido escasamente evaluado (12, 13), en referencia a esto Taft y cols. (14) validaron recientemente un cuestionario para evaluar el impacto de la enfermedad en la calidad de vida de los pacientes (EoO-QOL-A).
Es sabido, que debido al impacto psicosocial de la enfermedad, los pacientes adoptan mecanismos de defensa en el momento de la deglución que enmascaran los síntomas durante la anamnesis (15) y dificultan el diagnóstico y el seguimiento de la enfermedad. Dada la ausencia de Scores en población adulta capaces de medir la afectación clínica, resulta difícil monitorizar las variaciones en el espectro de síntomas que provocan los distintos tratamientos en función de la respuesta a los mismos.
El objetivo de nuestro estudio, es evaluar la utilidad de Índice ELSA en la monitorización de la actividad clínica de la enfermedad en función de su respuesta o no a tratamiento con inhibidores de la bomba de protones (IBPs) + dietas (dieta de exclusión selectiva según test de alergia (SED) y dieta de exclusión de 6 familias alimentos basada en la publicada por Kagalwalla y cols (16) (SFED)). También estudiamos la correlación existente entre la puntuación del Score y los parámetros de actividad del eosinófilo (eosinófilos en suero, proteína catiónica del eosinófilo (ECP) en suero e IgE total), así como con el recuento de eosinófilos en las biopsias de esófago.
MATERIAL Y MÉTODOS
Diseño de Índice EoE Live Symptoms Assessment (ELSA)
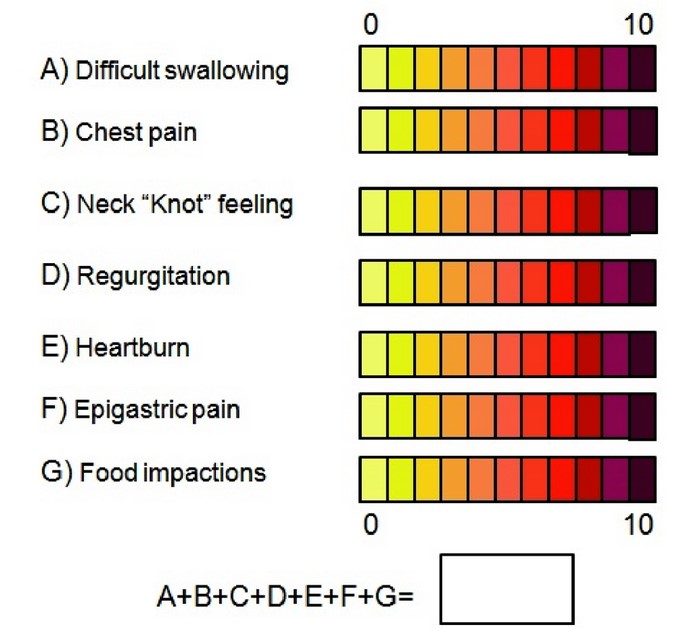
La escala visual analógica (VAS), es el método de evaluación subjetiva de síntomas más usado en la práctica clínica, dentro de este test hemos utilizado un subtipo de VAS denominado Escala numérica, que consiste en un conjunto de números de cero a diez, donde cero es la ausencia del síntoma a evaluar y diez su mayor intensidad. Se pide al paciente que seleccione el número que mejor indique la intensidad del síntoma que se está evaluando. Índice ELSA consta de 7 ítems que corresponden con los 7 síntomas más frecuentes de EoE en población adulta definidos por consenso entre expertos en la enfermedad siguiendo una metodología Delphi. Los síntomas seleccionados fueron los siguientes: (A) dificultad para deglutir, (B) dolor torácico, (C) sensación de nudo cervical, (D) regurgitaciones, (E) sensación de pirosis, (F) dolor epigástrico, (G) Impactaciones con alimentos. Cada uno de estos síntomas es puntuado del 0 al 10 según una escala visual analógica. Se suman cada una de las puntuaciones obteniendo un total de 0 a 70 puntos (Figura 1).

Figura 1. Índice ELSA
Diseño del estudio
Se diseñó un estudio prospectivo, longitudinal y analítico sobre una cohorte de pacientes diagnosticados de EoE desde mayo hasta agosto de 2012. A dichos pacientes se les sometió a tratamiento con omeprazol 40 mg cada 24 horas + SED + SFED durante 6 semanas y posteriormente se sometieron a esofagoscopia con toma de biopsias de esófago para comprobar la respuesta histológica a tratamiento, dividiendo la muestra en respondedores (R) (<15 eo/cga) y no respondedores (NR) (≥15 eo/cga). Se determinó la puntuación del Score, niveles de IgE total (KU/L), proteína catiónica del eosinófilo (ECP) (mcg/ml), eo en suero (u/L), pico de eo/cga en las biopsias pre-tratamiento (basal) y post-tratamiento.
Se analizaron las diferencias existentes entre la cohorte de R y la de NR en cuanto a la puntuación global del Score Pretratamiento y postratamiento, así como las variaciones detectadas en los diferentes ítems.
Se estudió la existencia correlación entre la puntuación obtenida en el Score y los valores de Eo/cga en las biopsias, IgE total, ECP en suero y Eo/ml en suero. La puntuación basal del Score obtenida por pacientes con EoE se comparó con la obtenida por un grupo de controles sanos.
Selección de Pacientes
Se incluyeron en el estudio 20 pacientes diagnosticados de EoE desde mayo a agosto de 2012 pertenecientes al registro del Eosinophilic Esophagitis Research group del Hospital General Universitario de Ciudad Real-Hospital Gutierrez Ortega de Valdepeñas. Como grupo control se incluyeron 20 voluntarios sanos.
Análisis Estadístico
Se construyó una base de datos con el paquete estadístico PASW statistic 18 (IBM, Chicago, IL). Al tratarse de una muestra no paramétrica se utilizaron los test U de Mann-Whitney y rangos de Wilcoxon para variables continuas y χ2 para variables categóricas. Para la correlación de variables continuas se utilizó el test de Rho de Spearman. Se ha establecido la significación estadística cuando α ≤0.05.
Aspectos éticos
El estudio fue evaluado y aprobado por el Comité de Ética e Investigación Clínica (CEIC) del Hospital General Universitario de Ciudad Real. Los sujetos participantes firmaron un consentimiento informado previa inclusión en el estudio.
RESULTADOS
20 pacientes diagnosticados de EoE (80% varones; edad media 32,1 años ±12,38), fueron comparados con 20 controles sanos (60% varones; edad media 35,75 ± 12,45) (Tabla I). En cuanto a la puntuación basal de ELSA, no encontramos diferencias entre varones y mujeres, ni en cuanto a la edad. Si analizamos ambos grupos de forma independiente, el grupo EoE obtuvo una puntuación significativamente mayor que el grupo control (18,7 vs. 3,81; p<0,000) (Gráfico 1). Si estudiamos cada uno de los síntomas de forma individualizada, observamos que el grupo EoE obtuvo una puntuación significativamente mayor que grupo control en todos los ítems excepto en (D) (EoE 3,35 vs. Control 1,15; p=ns) y (E) (EoE 3,10 vs. Control 1,9; p=ns), en los que ambos grupos se comportaban de forma similar (Tabla I).
| Variables | EoE (n=20) | Controles (n=20) | p value |
| Sex (male) | 80% | 60% | ns |
| Age | 32,10 ±12,38 | 35,75 ± 12,45 | ns |
| Familiar Atopic history | 70,6% | 29,4% | 0,02 |
| Atopic | 100% | 0% | <0,000 |
| Food Allergies | 95% | 0% | <0,000 |
| Serum Eo (u/mL) | 395 ± 223,54 | 180,36 ± 141,26 | 0,001 |
| Índice ELSA (basal) | 18,7 | 3,81 | <0,000 |
| A (Disphagia) | 6,35 | 0,15 | <0,000 |
| B (Chest pain) | 2 | 0,05 | <0,000 |
| C (Neck knot feeling) | 5,4 | 0,2 | <0,000 |
| D (Regurgitation) | 3,35 | 1,15 | ns |
| E (Heartburn) | 3,10 | 1,9 | ns |
| F (Epigastric pain) | 2,55 | 0,55 | 0,006 |
| G (Food impactions) | 6,40 | 0 | <0,000 |

Gráfico 1. Puntuación de Índice ELSA R/NR comparado con grupo Control.
Se compararon las puntuaciones pre y posttratamiento obtenidas por 13 pacientes respondedores a tratamiento (R), frente a las obtenidas por 7 pacientes no respondedores (NR), siendo estas dos poblaciones homogéneas (Tabla II). Previamente a recibir tratamiento, ambos grupos presentaban similares puntuaciones tanto de forma global (R 30,08 vs. NR 26,86; p=0,52), como diferenciadas por síntomas. Si analizamos cual es el síntoma que más afecta a los pacientes, nos encontramos que la (D) es que más puntuación obtiene en el grupo de R (R 6,77 vs. NR 5,71; p=ns), mientras que (A) (R 6,38 vs. NR 6,29; p=ns) es el que más puntuación obtiene en NR. El dolor torácico (B), es el síntomas que presenta menor puntuación en ambos grupos (R 2,69 vs. NR 0,71; p=ns) (Tabla III).
| Variables | R (n=13) | NR (n=7) | p value |
| Sex (male) | 76,9% | 85,7% | ns |
| Age | 31,69 ±12,39 | 32,86±13,32 | ns |
| Atopic | 76,9% | 85,7% | ns |
| Serum Eo levels (u/mL) | 353,84 ± 185,36 | 471,42 ± 281,15 | ns |
| IgE levels (KU/L) | 418,12 ± 381,8 | 363,22 ± 275,51 | ns |
| Serum ECP levels (mcg/mL) | 30,09 ±15,67 | 38,92 ± 24,49 | ns |
| Peak Eo (u/hpf) Pretreatment | 38,15 ± 10,45 | 32,14 ± 15,97 | ns |
| Peak Eo (u/hpf) Posttreatment | 2,31 ± 2,86 | 42,14 ± 27,05 | ns |
| ELSA | R (n=13) / NR (n=7) | PreT | PostT | p value |
| A (0-10) | R | 6,38 | 0,2 | 0,001 |
| NR | 6,29 | 2,71 | 0,027 | |
| B (0-10) | R | 2,69 | 0,46 | 0,011 |
| NR | 0,71 | 0,57 | ns | |
| C (0-10) | R | 5,08 | 0,92 | 0,003 |
| NR | 6 | 3,57 | 0,042 | |
| D (0-10) | R | 3,46 | 0,62 | 0,011 |
| NR | 3,14 | 2,71 | ns | |
| E (0-10) | R | 3,23 | 0,69 | 0,003 |
| NR | 2,86 | 1,14 | ns | |
| F (0-10) | R | 2,77 | 0,38 | 0,007 |
| NR | 2,14 | 0,86 | ns | |
| G (0-10) | R | 6,77 | 1,08 | 0,002 |
| NR | 5,71 | 2,57 | ns | |
| Global (0-70) | R | 30,08 | 5,08 | 0,001 |
| NR | 26,86 | 14,14 | 0,018 |
Cuando analizamos, como influyó la respuesta al tratamiento en la puntuación obtenida en el Score tras la realización del mismo, se observó como en el grupo de R, se produjo mejoría significativa en cada uno de los ítems, siendo (A) (PreT 6,38 vs. PostT 0,2; p=0,001) y (G) (PreT 6,77 vs. PostT 1,08; p=0,002) los síntomas que mayor mejoría experimentaron, siendo (B) el que menos mejoró tras el tratamiento (2,69 vs. 0,46; p=0,01). En el grupo de NR, tan sólo se detectó mejoría significativa en (A) (PreT 6,29 vs. PostT 2,71; p=0,02) y en (C) (PretT 6 vs. PostT 3,59; p=0,04), en el resto de ítems (B, D, E, F, G) la mejoría no fue estadísticamente relevante (gráfico 2 y Tabla III).

Gráfico 2. Puntuaciones en Índice ELSA pre y post tratamiento en R y NR
En cuanto a la relación de ELSA con los hallazgos endoscópicos, encontramos que el grupo de R presentó un porcentaje mayor de normalización de la endoscopia tras tratamiento en comparación con el grupo de NR (R 76,9% vs. NR 28,6%; p=0,035 OR=8,33 95%CI (1,03-66,6)). Sin embargo, a pesar de que la puntuación obtenida en ELSA por pacientes con hallazgos patológicos fue superior a la obtenida por aquellos con endoscopia normal, esta diferencia no alcanzó la significación estadística (10,63 vs. 6,67; p=0,32).
En cuanto a los marcadores serológicos de actividad del eosinófilo, no se detectó una correlación significativa entre la puntuación obtenida en ELSA y los niveles de IgE total, ECP y el recuento de eosinófilos en suero, pre y post tratamiento, tanto en R como en NR: ELSA pretratamiento/Eo en suero (u/L)= R2 0,01; p=ns, IgE total (KU/L) R2=0,1;p=ns, ECP (mcg/ml) R2=0,061; p=ns. ELSA posttratamiento/Eo en suero (u/L) R2= 0,18; p=ns, IgE total (KU/L) R2= – 0,25; p=ns, ECP (mcg/ml) R2=0,31; p=ns.
Se relacionó el número de Eo/cga con ELSA pre y postratamiento sin obtener una correlación significativa, tanto en R como en NR. Pretratamiento ELSA/pico eo/cga: R2=0,08; p=ns. Posttratamiento ELSA /pico eo/cga: R2=0,1; p=ns).
DISCUSIÓN:
El manejo clínico de la EoE es algo poco consensuado, ya que no existen intervalos de seguimiento establecidos, ni herramientas que nos permiten establecer el grado de afectación clínica de los pacientes. Es interesante, profundizar en la búsqueda de parámetros clínicos y analíticos que ayuden a predecir periodos de reactivación de la enfermedad sin necesidad de tomar biopsias, ya que esto es un procedimiento costoso y cruento para el paciente (17). En esta línea, ELSA aporta más información a cerca de la monitorización clínica de la enfermedad, que unido a parámetros analíticos de actividad del eosinófilo servirían de gran ayuda para valorar la respuesta a los diferentes tratamientos.
La escala visual analógica (VAS), es el método de evaluación subjetiva de síntomas más frecuentemente utilizado y que ya ha sido testado en patología esofágica (18, 19) fundamentalmente en el contexto de ERGE. Dentro del contexto de evaluación de síntomas en la EoE, no existen métodos específicos para la enfermedad, por lo que se han usado Scores de Disfagia que obvian otros síntomas de importancia dentro de la clínica de la enfermedad, como son el reflujo, dolor torácico y sensación de impactación con alimentos, que los pacientes refieren como “stop” de los alimentos a nivel retroesternal.
Lucendo y cols. (20) publicaron un estudio donde demostraron la ineficacia de montelukast en el mantenimiento de la remisión de EoE en pacientes tratados con corticoides, para el seguimiento clínico de los pacientes, utilizaron un Score de Acalasia, publicado y validado previamente por Zaninotto y cols. (21), en dicho Score se evalúan tres síntomas: disfagia, pirosis y regurgitaciones cada uno de ellos puntuado del cero al tres dependiendo de la severidad de los síntomas. A la luz de la variedad de síntomas que componen la clínica de EoE, este Score tan sólo evalúa una parte de ellos, otros síntomas recogidos en la guía de consenso de 2011 (3) como la impactación con sólidos, el dolor epigástrico y el dolor torácico quedan sin monitorizar. Este hecho es de vital importancia ya que del 33% al 54% de los pacientes con EoE sufren impactaciones con alimentos que requieren tratamiento endoscópico (22) y en otras series publicadas, el dolor torácico supone el segundo síntoma más frecuente (23, 24). Referente a esto, Joo y cols. (25) publicaron un estudio recientemente donde diagnosticaron EoE en el 6,6% de pacientes que presentaban síntomas digestivos altos. En otro estudio, el 25% de los pacientes con EoE presentaba dolor abdominal asociado a los síntomas de disfunción esofágica (26), similares resultados obtuvieron Muller y cols (27). En nuestra serie, la “dificultad para deglutir” (disfagia) y la impactación con sólidos presentan puntuaciones medias similares, 6,35 y 6,40 respectivamente, siendo estos síntomas los de mayor valoración en el Score. Llama la atención, como “sensación de nudo cervical” obtiene puntuaciones superiores a pirosis y regurgitación: 5,4, 3,10 y 3,35 respectivamente, siendo el dolor torácico el síntoma con menor relevancia clínica (Tabla I). Otro Score usado para monitorizar la actividad clínica de la enfermedad es el utilizado por Gonsalves y cols. (28) en el que estudia únicamente la disfagia, monitorizando su intensidad, duración, frecuencia e impacto en la calidad de vida, siendo este efectivo en la monitorización de la actividad clínica de la enfermedad.
Cuando comparamos la puntuación obtenida en ELSA en pacientes con EoE y controles sanos, detectamos que todos los parámetros excepto pirosis y regurgitaciones son significativamente superiores en pacientes con EoE, esto puede ser debido a la alta prevalencia de clínica de reflujo en población general.
Llama la atención, como se produce un descenso significativo de la puntuación en el Score tanto en pacientes R como NR, hecho que también es observado en el estudio de Gonsalves y cols (28), donde se produce una respuesta clínica (mejoría en el Score de Disfagia) en el 94% de los pacientes mientras que la tasa de remisión histológica es del 70%, algo similar es observado por Kagalwalla y cols. (16) en población pediátrica. No tenemos explicación para este hecho, pero es posible que el efecto placebo o el tratamiento concomitante con IBP puedan explicar esta mejoría clínica. Es sabido que existe un subgrupo de pacientes con síntomas típicos de EoE, en los que se ha descartado ERGE y que presentan respuesta clínica e histológica al tratamiento con IBP (24), el término usado para describir este subtipo es EoE respondedora a IBP (3, 29), hecho que no hemos contemplado en el análisis, lo cual supone una limitación en nuestro estudio, sería necesario estudiar la puntuación del test en pacientes que reciben IBP y compararlo con aquellos que no lo reciben para comprobar esta hipótesis.
La búsqueda de marcadores serológicos de actividad de la enfermedad nos hizo analizar la correlación del Score con los parámetros de actividad del eosinófilo y el recuento de eosinófilos en las biopsias de esófago. En base a esto, recientemente Subbarao y cols. (30) comprobaron como los niveles séricos de Neurotoxina derivada del eosinófilo (EDN) se correlacionaba con la actividad clínica de la enfermedad, siendo a la vez superiores a los hallados en un grupo control. Este hecho ya fue constatado por Konikoff y cols. (31)
En nuestra experiencia, hemos observado como los niveles séricos de eosinófilos en pacientes con EoE son muy superiores a los encontrados en controles sanos, el resto de parámetros (IgE total y ECP) no fueron medidos en el grupo control. Sin embargo, tanto los niveles de eosinófilos en suero, como los niveles de IgE total y ECP no se correlacionaron con la respuesta a tratamiento siendo similares pre y post tratamiento en R y NR. Cuando estudiamos la relación de estos con la puntuación del Score mediante el test de Rho de Spearman, no encontramos correlación estadísticamente significativa. Esto contrasta con otros estudios, en los que se aprecian niveles altos de eosinófilos en suero en un 67% de pacientes con EoE (>15 eo/cga), disminuyendo el porcentaje al 50% en aquellos con 5-15 eo/cga y al 35% en los que presentaban <5eo/cga en las biopsias de esófago (32). Esta correlación de los niveles séricos de eosinófilos con la clínica fue observada también por Konikoff y cols.(31) Sin embargo, el papel del recuento de eosinófilos en suero como marcador de actividad de EoE es controvertido ya que aun quedan aspecto por resolver como son (17): establecer un punto de corte específico para la enfermedad, correlacionar los niveles con la existencia de enfermedades atópicas concomitantes, variabilidad estacional a causa de alérgenos respiratorios y su correlación con el recuento de eosinófilos en las biopsias de esófago.
En cuanto a IgE total, se han descrito niveles elevados del 4% al 69% de los adultos con EoE (17, 32, 33), pero su papel como marcador de actividad de la enfermedad es controvertido, ya que nuevamente su variabilidad estacional juega un papel importante en este aspecto, lo cual es posible que pueda influir en la historia clínica de la enfermedad, de hecho Wang y cols. (34) reportaron una menor incidencia de EoE en población infantil en los meses de invierno comparado con otras estaciones, hecho que fue constatado por Almansa y cols. (35)
En cuanto a ECP en suero, no hemos encontrado estudios que evalúen su papel como marcador de actividad de EoE. Teniendo en cuenta que la prevalencia de alergias alimentarias elevada en estos pacientes (95% en nuestra serie), Schwab y cols. (36) comprobaron como pacientes con alergias alimentarias presentaban niveles elevados de ECP en aspirado de íleon terminal en comparación con controles sanos. Centrándonos en EoE, recientemente Furuta y cols.(37) han publicado un interesante trabajo, donde determinan los niveles de ECP en secreciones intraluminales de esófago mediante un sistema denominado Enterotest, correlacionándose estos con el recuento de eosinófilos en las biopsias. Todo ello no concuerda con lo hallado en nuestro estudio, ya que a la luz de los resultados, ECP en suero no marca la actividad de la enfermedad, manteniéndose en niveles elevados en NR, por lo tanto no se correlaciona con la puntuación de ELSA, se requieren más estudios que evalúen de forma prospectiva y secuencial los niveles de ECP en pacientes que se mantienen en remisión en periodos superiores a 6 semanas. En cuanto a la relación de ELSA con el recuento de eosinófilos en las biopsias de esófago, encontramos una débil correlación postratamiento, que no llegó a ser estadísticamente significativa, a diferencia de lo publicado por Pemtiuk y cols. (7), que sí encuentran una débil correlación positiva entre el recuento de eosinófilos en las biopsias y la puntuación en el score PEESS versión 1.0.
En conclusión, ELSA supone el primer Score específico de EoE en adultos lo cual proporciona una herramienta eficaz en la monitorización de la actividad de la enfermedad, que nos permite cuantificar el impacto clínico de cada uno de los síntomas. A su vez nos permite valorar variaciones de estos, según la respuesta a los distintos tratamientos. A la luz de nuestros resultados, el recuento de eosinófilos en suero, IgE total y ECP sérica no se comportan como marcadores de actividad de EoE y por tanto sus valores no se correlacionan con la puntuación en ELSA. No obstante, es necesario testar como se comporta ELSA sobre una muestra mayor y analizar su utilidad en el seguimiento a largo plazo de los pacientes, evaluando su capacidad para detectar recaidas durante periodos de remisión.
REFERENCES
- Arias A, Lucendo AJ. Prevalence of eosinophilic oesophagitis in adult patients in a central region of Spain. Eur J Gastroenterol Hepatol 2012 Oct 16.
- Katzka DA. Demographic data and symptoms of eosinophilic esophagitis in adults. Gastrointest Endosc Clin N Am 2008 Jan;18(1):25-32; viii.
- Liacouras CA, Furuta GT, Hirano I, Atkins D, Attwood SE, Bonis PA, et al. Eosinophilic esophagitis: Updated consensus recommendations for children and adults. J Allergy Clin Immunol 2011 Apr 6.
- Mackenzie SH, Go M, Chadwick B, Thomas K, Fang J, Kuwada S, et al. Eosinophilic oesophagitis in patients presenting with dysphagia–a prospective analysis. Aliment Pharmacol Ther 2008 Nov 1;28(9):1140-6.
- Prasad GA, Talley NJ, Romero Y, Arora AS, Kryzer LA, Smyrk TC, et al. Prevalence and predictive factors of eosinophilic esophagitis in patients presenting with dysphagia: a prospective study. Am J Gastroenterol 2007 Dec;102(12):2627-32.
- Mukkada VA, Haas A, Maune NC, Capocelli KE, Henry M, Gilman N, et al. Feeding dysfunction in children with eosinophilic gastrointestinal diseases. Pediatrics 2010 Sep;126(3):e672-7.
- Pentiuk S, Putnam PE, Collins MH, Rothenberg ME. Dissociation between symptoms and histological severity in pediatric eosinophilic esophagitis. J Pediatr Gastroenterol Nutr 2009 Feb;48(2):152-60.
- Franciosi JP, Hommel KA, DeBrosse CW, Greenberg AB, Greenler AJ, Abonia JP, et al. Development of a validated patient-reported symptom metric for pediatric eosinophilic esophagitis: qualitative methods. BMC Gastroenterol 2011;11:126.
- Dellon ES, Gibbs WB, Fritchie KJ, Rubinas TC, Wilson LA, Woosley JT, et al. Clinical, endoscopic, and histologic findings distinguish eosinophilic esophagitis from gastroesophageal reflux disease. Clin Gastroenterol Hepatol 2009 Dec;7(12):1305-13; quiz 261.
- Rodríguez -Sánchez J, López Viedma B, Martín Dávila F, Lorente Poyatos R, Hernández Albujar A, Rodríguez Sánchez E. La esofagitis eosinofílica como causa de impactación por cuerpo extraño. Análisis de nuestra experiencia. Apunt Cienc 2011;3:20-8.
- Mulder DJ, Hurlbut DJ, Noble AJ, Justinich CJ. Clinical Features Distinguish Eosinophilic And Reflux-Induced Esophagitis: An Age-Matched, Case-Controlled Study And A Novel Scoring System. J Pediatr Gastroenterol Nutr 2012 Oct 18.
- Klinnert M, Moore W, Atkins D, Fleischer D, Furuta G. Impact of eosinophilicesophagitis on quality of life for youth and their families. J Allergy Clin Immunol Allergy Clin North Am 2011;127:AB106.
- Gonsalves N, Hirano I. Quality of life assessment in adults with EoE at baseline and after treatment with dietary therapy: is the treatment worse than the disease? Gastroenterology 2009;136:A137.
- Taft TH, Kern E, Kwiatek MA, Hirano I, Gonsalves N, Keefer L. The adult eosinophilic oesophagitis quality of life questionnaire: a new measure of health-related quality of life. Aliment Pharmacol Ther 2011 Oct;34(7):790-8.
- Dellon ES. Eosinophilic esophagitis: diagnostic tests and criteria. Curr Opin Gastroenterol 2012;28:382-8.
- Kagalwalla AF, Sentongo TA, Ritz S, Hess T, Nelson SP, Emerick KM, et al. Effect of six-food elimination diet on clinical and histologic outcomes in eosinophilic esophagitis. Clin Gastroenterol Hepatol 2006 Sep;4(9):1097-102.
- Gupta SK. Noninvasive markers of eosinophilic esophagitis. Gastrointest Endosc Clin N Am 2008 Jan;18(1):157-67; xi.
- Yang M, Li ZS, Chen DF, Zou DW, Xu XR, Fang DC, et al. Quantitative assessment and characterization of visceral hyperalgesia evoked by esophageal balloon distention and acid perfusion in patients with functional heartburn, nonerosive reflux disease, and erosive esophagitis. Clin J Pain 2010 May;26(4):326-31.
- Savarino E, de Bortoli N, Zentilin P, Martinucci I, Bruzzone L, Furnari M, et al. Alginate controls heartburn in patients with erosive and nonerosive reflux disease. World J Gastroenterol 2012 Aug 28;18(32):4371-8.
- Lucendo AJ, De Rezende LC, Jimenez-Contreras S, Yague-Compadre JL, Gonzalez-Cervera J, Mota-Huertas T, et al. Montelukast was inefficient in maintaining steroid-induced remission in adult eosinophilic esophagitis. Dig Dis Sci 2011 Dec;56(12):3551-8.
- Zaninotto G, Costantini M, Molena D, Buin F, Carta A, Nicoletti L, et al. Treatment of esophageal achalasia with laparoscopic Heller myotomy and Dor partial anterior fundoplication: prospective evaluation of 100 consecutive patients. J Gastrointest Surg. 2000 May-Jun;4(3):282-9.
- Desai TK, Stecevic V, Chang CH, Goldstein NS, Badizadegan K, Furuta GT. Association of eosinophilic inflammation with esophageal food impaction in adults. Gastrointest Endosc 2005 Jun;61(7):795-801.
- Poh CH, Gasiorowska A, Navarro-Rodriguez T, Willis MR, Hargadon D, Noelck N, et al. Upper GI tract findings in patients with heartburn in whom proton pump inhibitor treatment failed versus those not receiving antireflux treatment. Gastrointest Endosc 2010 Jan;71(1):28-34.
- Molina-Infante J, Ferrando-Lamana L, Ripoll C, Hernández-Alonso M, Mateos JM, Fernández-Bermejo M, et al. Esophageal eosinophilic infiltration responds to proton pump inhibition in most adults. Clin Gastroenterol Hepatol 2011 Feb;9(2):110-7.
- Joo MK, Park JJ, Kim SH, Kim KH, Jung W, Yun JW, et al. Prevalence and endoscopic features of eosinophilic esophagitis in patients with esophageal or upper gastrointestinal symptoms. J Dig Dis 2012 Jun;13(6):296-303.
- Shi YN, Sun SJ, Xiong LS, Cao QH, Cui Y, Chen MH. Prevalence, clinical manifestations and endoscopic features of eosinophilic esophagitis: a pathological review in China. J Dig Dis 2012 Jun;13(6):304-9.
- Muller S, Puhl S, Vieth M, Stolte M. Analysis of symptoms and endoscopic findings in 117 patients with histological diagnoses of eosinophilic esophagitis. Endoscopy 2007 Apr;39(4): 339-44.
- Gonsalves N, Yang GY, Doerfler B, Ritz S, Ditto AM, Hirano I. Elimination Diet Effectively Treats Eosinophilic Esophagitis in Adults; Food Reintroduction Identifies Causative Factors. Gastroenterology 2012 Mar 2.
- Dohil R, Newbury RO, Aceves S. Transient PPI responsive esophageal eosinophilia may be a clinical sub-phenotype of pediatric eosinophilic esophagitis. Dig Dis Sci 2012 May;57(5): 1413-9.
- Subbarao G, Rosenman MB, Ohnuki L, Georgelas A, Davis M, Fitzgerald JF, et al. Exploring potential noninvasive biomarkers in eosinophilic esophagitis in children. J Pediatr Gastroenterol Nutr 2011 Dec;53(6):651-8.
- Konikoff MR, Blanchard C, Kirby C, Buckmeier BK, Cohen MB, Heubi JE, et al. Potential of blood eosinophils, eosinophil-derived neurotoxin, and eotaxin-3 as biomarkers of eosinophilic esophagitis. Clin Gastroenterol Hepatol 2006 Nov;4(11):1328-36.
- Baxi S, Gupta SK, Swigonski N, Fitzgerald JF. Clinical presentation of patients with eosinophilic inflammation of the esophagus. Gastrointest Endosc 2006 Oct;64(4):473-8.
- Remedios M, Campbell C, Jones DM, Kerlin P. Eosinophilic esophagitis in adults: clinical, endoscopic, histologic findings, and response to treatment with fluticasone propionate. Gastrointest Endosc 2006 Jan;63(1):3-12.
- Wang FY, Gupta SK, Fitzgerald JF. Is there a seasonal variation in the incidence or intensity of allergic eosinophilic esophagitis in newly diagnosed children? J Clin Gastroenterol 2007 May-Jun;41(5):451-3.
- Almansa C, Krishna M, Buchner AM, Ghabril MS, Talley N, DeVault KR, et al. Seasonal distribution in newly diagnosed cases of eosinophilic esophagitis in adults. Am J Gastroenterol 2009 Apr;104(4):828-33.
- Schwab D, Raithel M, Klein P, Winterkamp S, Weidenhiller M, Radespiel-Troeger M, et al. Immunoglobulin E and eosinophilic cationic protein in segmental lavage fluid of the small and large bowel identify patients with food allergy. Am J Gastroenterol 2001 Feb;96(2):508-14.
- Furuta GT, Kagalwalla AF, Lee JJ, Alumkal P, Maybruck BT, Fillon S, et al. The oesophageal string test: a novel, minimally invasive method measures mucosal inflammation in eosinophilic oesophagitis. Gut 2012 Aug 15.
